生命科学与技术学院岳锐/徐大春团队等合作揭示Fap调控心肌梗死修复的新机制,相关研究成果发表于《循环研究》
来源:生命科学与技术学院
时间:2023-02-20 浏览:
2月9日,同济大学生命科学与技术学院、附属东方医院再生医学研究所岳锐课题组联合同济大学附属第十人民医院徐大春课题组、上海交通大学医学院附属新华医院张力课题组在国际著名期刊《循环研究》(Circulation Research)在线发表了题为“Inhibition of Fap Promotes Cardiac Repair by Stabilizing BNP”的研究论文。该研究系统阐明了Fap调控心肌梗死损伤修复的作用及分子机制,发现抑制Fap能够通过稳定脑利钠肽(Brain natriuretic peptide,BNP)蛋白水平促进血管新生和心脏修复,从而为该类疾病的临床诊断、预后和治疗提供了新思路与新靶点。

急性心肌梗死是最常见的致死原因之一,发病率居高不下,严重威胁人类健康。急性心肌梗死发生后,心脏成纤维细胞(Cardiac fibroblasts,CFs)主要参与了损伤修复过程。然而,CFs具有较强的异质性,部分CFs特异性高表达成纤维细胞激活蛋白(Fibroblast activation protein,Fap),作为一种丝氨酸蛋白酶,Fap在活化的成纤维细胞中显著上调,并在细胞外基质降解、肿瘤微环境形成、炎症和伤口愈合中发挥关键调控作用。但是,心肌梗死后Fap是否参与心脏损伤修复尚不清楚。既往研究表明,通过嵌合抗原受体T细胞免疫疗法(Chimeric Antigen Receptor T-Cell Immunotherapy,CAR-T)清除心脏损伤后的Fap+ CFs可以显著改善心脏功能,减少心肌纤维化,但是,值得关注的是,岳锐课题组的前期研究发现Fap在骨髓基质细胞和成骨细胞中同样高表达,因此,通过CAR-T疗法系统性清除此类细胞会导致严重的贫血、骨量减少、体重下降及恶病质状态。
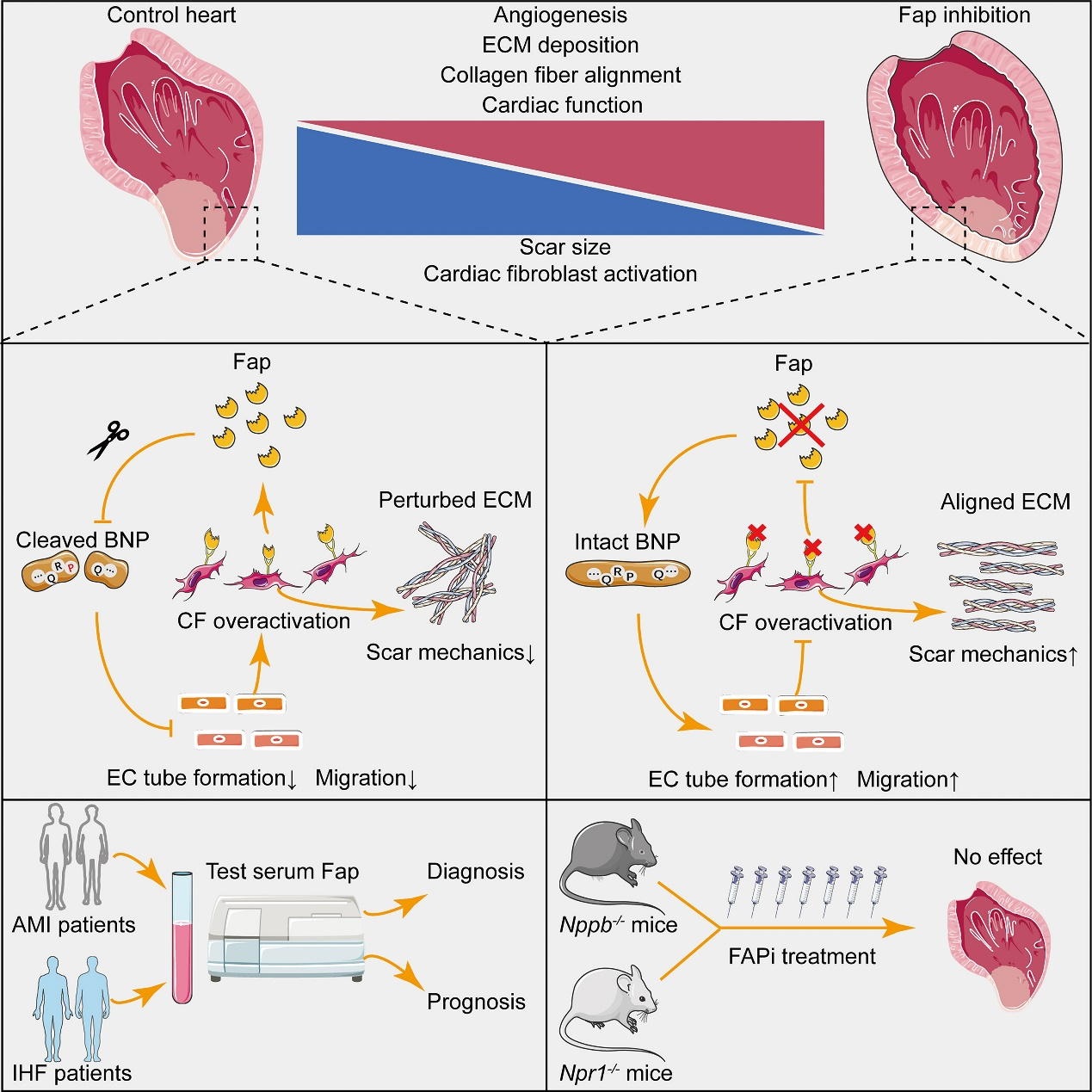
研究人员首先分析了肥厚性心肌病、缺血性心力衰竭患者的心肌组织样本,免疫荧光及蛋白印迹实验发现Fap在此类患者的心肌组织中表达量明显升高。为了进一步探究Fap在心肌梗死后损伤修复过程中的作用,研究者通过基因敲除Fap或药物抑制Fap酶切活性,构建了Fap功能失活的动物模型,随后的心超检查及组织学分析显示,Fap功能失活后心肌梗死小鼠的心脏功能更好,小鼠心肌梗死疤痕面积更小,梗死边缘区α-SMA+及Postn+的心脏成纤维细胞更少,提示成纤维细胞活化减少。与此同时,抑制Fap后小鼠心肌梗死边缘区血管生成增多,胶原纤维排列更整齐致密,提示抑制Fap可促进小鼠心肌梗死后的损伤修复。
为进一步阐明抑制Fap后促进心脏修复的具体分子机制,研究者对敲除Fap、抑制Fap及野生型小鼠心肌梗死后的心脏组织进行RNA-Seq,测序结果发现敲除和抑制Fap后可显著增强心肌收缩力、促进ECM在心肌梗死边缘区分泌及沉积,并显著上调HIF 1α、cGMP-PKG信号通路。有趣的是,BNP是激活cGMP-PKG信号通路的重要因子,研究者通过体外蛋白共孵育实验发现BNP可以被Fap切割降解,提示BNP是Fap潜在的酶切底物。随后的细胞实验证明,Fap可以抑制BNP促进ECs成管、迁移的生物学功能。为了进一步探索BNP是否为Fap的内源性底物,研究者构建了BNP或其受体(Npr1)敲除小鼠,在这类小鼠中进一步敲除或抑制Fap则无法发挥相应的保护作用,表明BNP/Npr1-cGMP-PKG通路介导了抑制Fap后的心脏保护作用。
综上所述,该研究揭示了Fap在心肌梗死后损伤修复中的关键作用,并阐明了其具体分子机制。由于BNP已被广泛应用于临床心力衰竭的诊断及治疗中,围绕BNP/Npr1-cGMP-PKG通路开发的多种新药已被FDA批准并应用于临床治疗,因此该研究具有巨大的转化价值,为未来心血管疾病的诊治提供了新思路和新靶点。
该研究由同济大学生命科学与技术学院岳锐教授、同济大学附属第十人民医院徐大春教授及上海交通大学附属新华医院张力教授共同指导完成。上海交通大学附属新华医院孙玉玺博士、同济大学医学院马梦秋博士为论文共同第一作者。该研究工作得到了科技部重点研发计划、国家杰出青年科学基金、国家自然科学基金等多项基金的支持。
论文链接:https://www.ahajournals.org/doi/abs/10.1161/CIRCRESAHA.122.320781